سلام دوستان
تا حالا به آبی که هر روز بار ها با آن سرکار دارید دقیق نگاه کردید؟فکر نکنم!
گاهی اوقات خواندن چنین مطالبی به ما کمک میکنه که بدونیم اطرافمون چی میگذره؟
این متن رو درباره آب(به همین سادگی) جمع آوری کردم،بخونید و از دنیای شیمی لذت ببرید.
متن رو لطفا کامل بخونید وگرنه...
چرا آب، عجیبترین مایع جهان است؟
دانش - آب، فراوانترین مایع و بهجرات مهمترین مایعی است که روی زمین وجود دارد؛ اما اهمیت آن به پدیدههای زیستی منحصر نمیشود. ویژگیهای فیزیکی آب در مقایسه با دیگر مواد روی زمین، بینظیر است.
محمود حاجزمان: ما با معماهای زیادی مواجه هستیم، از طبیعت ماده تاریک و سر منشاء جهان گرفته، تا تحقیق برای نظریه همهچیز. اینها همه معماهایی در مقیاس بزرگ هستند، اما شما میتوانید معمای دیگری را از جهان فیزیکی مشاهده کنید که از آشپزخانه شما میآید (و اگر همانقدر بزرگ نباشد، به همان اندازه گیجکننده باشد). فقط یک لیوان را از آب سرد پر کنید، یک قالب یخ در آن بیاندازید و صبر کنید تا آب از تلاطم بیفتد
.
این واقعیت که یخ شناور میشود، اولین مورد عجیب این ماده است. زمانی معما عمیقتر میشود که با استفاده از یک دماسنج دمای آب را در اعماق مختلف اندازه بگیرید. در بالا و در نزدیک قالب یخ، میبینید که دمای آب نزدیک به صفر درجه است، اما در انتهای لیوان دما به 4 درجه میرسد. دلیل آن این است که چگالی آب در دمای 4 درجه سلسیوس، از هر دمای دیگری بیشتر است (یک ویژگی عجیب دیگر که آن را از هر مایع دیگری متمایز میسازد).
به گزارش نیوساینتیست، خواص عجیب آب همچنان ادامه دارد و برخی از آنها برای زندگی حیاتی هستند. به دلیل اینکه چگالی یخ از آب کمتر است و چگالی آب در نقطه انجماد کمتر از زمانی است که آب تا چهار درجه گرمتر باشد، آب نسبت به ته لیوان، از بالا به پایین منجمد میشود. بنابراین حتی در طول عصر یخ بندان، زندگی در اعماق دریاها و اقیانوسها همچنان ادامه داشت. آب ظرفیت خارقالعادهای برای گرفتن گرما دارد و این به ملایمتر کردن تغییرات آبو هوایی کمک میکند، که در غیر این صورت میتواند اکوسیستمها را نابود کند.
با این حال، به رغم اهمیت بسیار زیاد آب برای حیات، هیچ نظریه واحدی دست کم تا کنون نتوانسته یک توضیح قابل قبول برای خصوصیات اسرارآمیز آن ارائه کند. اگر ما بتوانیم نظریات اندرس نیلسون از فیزیکدانان دانشگاه استنفورد کالیفرنیا، و لارس پترسون از دانشگاه استکهلم سوئد، و همکاران این دو را بپذیریم؛ بالاخره توانستهایم به دلیل واقعی خیلی از این خصوصیات غیر عادی پی ببریم.
نظریات جنجالی این دو، بسط دهنده نظریهای است که بیش از یک قرن پیش از این توسط ویلهلم رونتگن، کاشف اشعه ایکس، ارائه شده است. او ادعا کرده بود که مولکولها در آب مایع آن گونه که در کتابهای امروزی میبینیم، تنها از یک طریق به هم نپیوستهاند، بلکه این اتصال از دو مسیر کاملا متفاوت انجام میشود.
ساختار اسرارآمیز آب
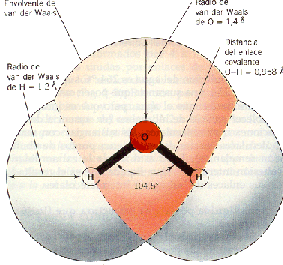
کلید فهم اسرار آب، نحوه تعامل مولکولهای آن با همدیگر است، مولکولهایی که از یک اتم اکسیژن و دو اتم هیدروژن تشکیل شدهاند. اتم اکسیژن بار منفی ناچیزی دارد و اتمهای هیدروژن، در مجموع بار مثبتی معادل آن دارند. به همین ترتیب، اتمهای هیدروژن و اکسیژن مولکولهای همسایه، از طریق تشکیل پیوندی به نام پیوند هیدروژنی به همدیگر جذب میشوند.
پیوندهای هیدروژنی، خیلی ضعیفتر از پیوندهایی هستند که اتمها را در مولکولها در کنار هم قرار میدهند، و به همین دلیل همواره در حال گسیختن و بازپیوستن هستند. این پیوندها هنگامی به حداکثر قدرت خود میرسند که مولکولها به نحوی کنار هم قرار گرفته باشند که هر پیوند هیدوژنی در امتداد یک پویند مولکولی قرار بگیرد. شکل یک مولکول آب به نحوی است که هر مولکول H2O در میان چهار مولکول همسایه قرار میگیرد و یک هرم با قاعده مثلثی را تشکیل میدهد، که معمولا به نام تتراهدرون یا چهارسطحی شناخته میشود.
دست کم، این راهی است که مولکولها در یخ در کنار هم قرار میگیرند. از یک دیدگاه متعارف سنتی، آب مایع یک ساختار مشابه ولی کمتر صلب دارد، که در آن مولکولهای بیشتری میتوانند در برخی از فضاهای خالی در یک آرایش چهار سطحی قرار بگیرند. این امر توضیح میدهد که چرا آب مایع از یخ چگالتر است، و به نظر میرسد که با نتایج آزمایشهای گوناگون که در آنها پرتوهای ایکس، فرو سرخ و نوترونها، از نمونههای آب منعکس میشوند همخوانی داشته باشد.
برخی از فیزیکدانها ادعا کردهاند که آبی که تحت شرایط به خصوصی قرار گرفته باشد، به دو ساختار کاملا متفاوت تجزیه میشود. ولی اکثر آنها چنین فرض میکنند که در شرایط عادی، تنها یک ساختار وجود دارد.
اما ده سال قبل، یک کشف اتفاقی توسط پترسون و نیلسون، این تصویر را به چالش کشید. آنها در حال استفاده از طیفسنجی جذبی اشعه ایکس برای تحقیق در مورد آمینو اسید گلیسین بودند. نقاط پیک در طیف جذبی اشعه ایکس میتواند ماهیت دقیق اتصالات شیمیایی ماده هدف را مشخص کنند، و همچنین به تعیین ساختار آن کمک کنند. نکته مهم این بود که آن دو از یک منبع جدید قدرتمند اشعه ایکس استفاده میکردند که میتوانستند با استفاده از آن، اندازهگیریهای حساستر و دقیقتری را نسبت به آن چه تا پیش از این ممکن بود انجام دهند. آنها به زودی دریافتند که آبی که حاوی نمونه گلیسین بود، طیف خیلی جالبتری به نسبت خود آمینو اسید تولید میکرد. نیلسون میگوید: «آنچه ما دیدیم بسیار شورانگیز بود، بنابراین ما احساس کردیم که باید به کنه آن پی ببریم».
مفاهیم مهیج
ویژگی که توجه آنها را جلب کرد یک نقطه پیک در طیف جذبی بود که توسط مدلهای سنتی آب مایع پیشبینی نشده بود. در حقیقت، در مقالهای که آنها در سال 2004 منتشر کردند چنین نتیجه گرفتند که در هر لحظه، 85 درصد از پیوندهای هیدروژنی در آب، باید تضعیف و یا شکسته شده باشند. این مقدار خیلی بیشتر از 10 درصدی است که توسط مدلهای کتب درسی پیشبینی شده است.
مفاهیم این یافته بسیار جالب توجه هستند: این به معنی آن است که یک بازنگری کامل در ساختار آب مورد نیاز است. در نتیجه نیلسون و پترسون شروع به انجام آزمایشهای دیگری با پرتو ایکس برای اثبات ادعای خود کردند. اولین حرکت آنها استقبال از کمک شیک شین از دانشگاه توکیو در ژاپن بود. وی متخصص تکنیکی است که «طیفسنجی نشری اشعه ایکس» نام دارد. نکته کلیدی در مورد این طیفسنجی این است که در طیف نشری یک ماده، هر چه طولموج اشعه ایکس کوتاهتر باشد، پیوند هیدروژنی باید ضعیفتر باشد.
نتیجه عالی بود: طیف اشعه ایکس نشری، شامل دو نقطه پیک بود که ممکن بود ناشی از دو ساختار جداگانه باشند. اعضای گروه چنین استدلال کردند که پیک مربوط به اشعههای ایکس با طولموج بلندتر، نشان دهنده سهم مولکولهایی است که به صورت چهار سطحی آرایش یافتهاند، در حالی که پیک طولموج کوتاهتر، بازتاب دهنده سهم مولکولهایی است که ساختار متفاوتی دارند.
جالب اینجا بود که پیک طولموج کوتاهتر در نشر اشعه ایکس شدیدتر از دیگری بود. این بدان معنی است که مولکولهای با پیوند ضعیفتر در آن نمونه، شایعتر بودند؛ و این خود تاییدی بر ادعای پیشین اعضای گروه بود. علاوه بر آن، آنها همچنین دریافتند که هر چه آب گرمتر باشد، این پیک به طولموجهای کوتاهتری منتقل میشود؛ در حالی که پیک دیگر، کمابیش ثابت باقی میماند.
این بدان معنی است که پیوندهای هیدروژنی اتصال دهنده مولکولهای موجود در این ساختار متفاوت، در اثر گرما بیشتر تضعیف میشوند؛ که باز هم با پیشبینیهای گروه مطابقت داشت. آنها سپس دادههای تجربی قدیمیتر را، که به نظر میرسید که با شکل سنتی آب مطابقت دارد، دوباره بررسی کردند و اکنون ادعا میکنند که این نتایج نیز با مدل جدید مطابقت دارد.
اگر آنها درست بگویند سوال دیگری مطرح میشود: تفاوتها در ساختارهای مختلف در مایع تا چه اندازه است؟ برای یافتن پاسخ، آنها از یک اشعه ایکس پرتوان استفاده کردند که در منبع نور تابشی سینکرترون دانشگاه استنفورد در کالیفرنیا تولید شده بود. این بار، چگونگی پراکندن پرتوهای ورودی از زاویههای مختلف به سطح آب، مورد ارزیابی واقع شدند. به گفته آنها، نتایج آشکار میکند که آب پوشیده از نواحی کوچکی از مولکولهایی است که به صورت چهار سطحی آرایش یافتهاند، و هر طول هر ناحیه نیز بین 1 تا 2 نانومتر است..
با ترکیب ای یافتهها با اندازهگیریهای دیگری که توسط اووه برگمن در دانشگاه استانفورد انجام شدهبود، آنها نتیجه گرفتند که ساختارهای منظم، که هر یک به طور متوسط شامل50 تا 100 مولکول هستند، توسط دریایی از پیوندهای مولکولی ضعیف احاطه شدهاند. ولی این نواحی ثابت نیستند. در کمتر از یک تریلیونیوم ثانیه، مولکولهای آب بین دو حالت گسست و باز تولید پیوندهای هیدروژنی نوسان میکنند.
توضیح غیر قابل توضیح!
توازن متغیر بین دو نوع آب که توسط نیلسون و پترسون مطرح شده بود، میتواند توضیحی باشد بر اینکه چرا آب در دمای 4 درجه به بیشترین چگالی خود میرسد. در نواحی آشفته مولکولهای آب به هم نزدیکتر هستند که این خود باعث چگالتر شدن آب نسبت به نواحی میشود که مولکولهای آب در ساختار چهار سطحی منظم آرایش داده شدهاند. در دمای صفر درجه نواحی آشفته نسبتا کمیاب هستند اما زمانی که آب گرمتر میشود، انرژی گرمایی اضافی تمایل بیشتری به لرزاندن و جدا کردن ساختارهای منظمتر مییابد. بنابراین مولکولها زمان کمتری را در ساختارهای منظم چهار سطحی و مدت زمان بیشتری را در نواحی آشفته سپری میکنند، امری که در مجموع باعث بیشتر شدن چگالی میشود.
از سوی دیگر، زمانیکه دما افزایش مییابد، حرکت مولکولهای با پیوند ضعیفتر بیشتر خواهد شد و همین مسئله بهتدریج آنها را وا میدارد که از هم دورتر شوند. این بسط که یک بار به توضیح دلیل چگالی بیشینه آب در دمای چهار درجه سلسیوس بالای صفر کمک کرده بود، این بار نیز به توضیح دلیل کاهش چگالی و افزایش حجم آب با افزایش بیشتر دمای آن کمک میکند.
به عقیده پترسون، این نظریه توضیحات کاملی را برای بسیاری از خواص غیرطبیعی غیر قابل توجیه دیگر آب ارائه میکند. مواردی که به ادعای آن دو، دیگر نظریهها هنوز نتوانستهاند به آن دست یابند. مارتین چاپلین، که یک شیمیدان در دانشگاه ساوث بنک لندن است، با این نظریه موافق است. توضیحاتی که بر مبنای سیستم تک مولفهای متعارف بودند، مجبور بودند زمانی که دمای آب تغییر میکند تلاش زیادی بکنند تا بتوانند ویژگیهای متعدد آب از قبیل کمینه و بیشینه را با نظریه خود سازگار کنند. چاپلین میگوید: «ساختار دوگانه کاملا با آزمایشها همخوانی دارد و میتواند خصوصیات غیر عادی آب را خیلی سادهتر از مدلهای سنتی توضیح دهد».
به مقاله سال 2004 نیلسون و پترسون در مجله ساینس تا کنون بیش از 350 بار و توسط محققین دیگر، ارجاع شده است. با این حال، هنوز خیلیها بدبین هستند. یک بدبینی این است که توضیح گروه در مورد نتایج طیفسنجی اشعه ایکس، بر مبنای شبیه سازی دست کم 50 مولکول آب در حال تعامل با هم است. یک مدل بینهایت پیچیده که تنها میتواند به طور تقریبی حل شود. ریچارد سایکالی از دانشگاه برکلی کالیفرنیا میگوید: «ما نیاز به یک نظریه خیلی دقیقتر داریم تا بتوانیم چنین ادعای بزرگی را بپذیریم». او ادعا میکند که تنظیمات کوچک برای آرایش پیوندهای هیدروژنی در ساختارهای متعارف، برای توضیح نتایج اشعه ایکس پترسون و نیلسون کفایت میکنند. حتی یکی از اعضای گروه آنها، مایکل اوبلیوس از دانشگاه استکهلم، همکاری خود را با آنها قطع کرد چرا که با تفسیر آنها از دادههای نشر اشعه ایکس موافق نبود.
یک نکته جزئی که خیلی از افراد را به این نظریه بدبین کرده بود، یک ادعا در مقاله سال 2004 بود که مولکولهایی که پیوند ضعیفتری دارند، تشکیل حلقه و زنجیره میدهند؛ و در واقع نیلسون و همکارانش نیز اکنون کمتر در مورد جزئیات ساختار مولکولی نامنظم اظهار نظر میکنند. ولی یوجین استنلی ازدانشگاه بوستون، باور ندارد که این امر کاملا نظریه آنها را زیر سوال میبرد: وی میگوید: «من فکر نمیکنم که آنها باید تا ابد محکوم شوند». به رغم این که نظریه آنها هنوز جای کار دارد، ولی به گفته او، نتایج پراکنش اشعه ایکس شواهدی بر تایید نظریه آنها ارائه میکند.
هیچ شکی نیست که هنوز نیلسون و پترسون با مخالفتهای شدیدی مواجه خواهند بود، ولی پاداشهای یک درک فراگیر از ساختار آب مایع میتواند شایان توجه باشد. این درک میتواند منجر به درک بهتر از مواردی مانند چگونگی برهمکنش پروتئینها و داروها با مولکولهای آب در بدن، و در نتیجه تولید داروهای موثرتری گردد. با دادن یک ایده بهتر از چگونگی رفتار مولکولهای آب در اطراف منافذ ریز ما، میتواند به تلاشها برای نمک زدایی و تصفیه آب کمک کند و سطح دسترسی به آب تمیز را بیشتر کند.
پترسون میگوید: «درک ما از آب یک تصویر در حال تکامل است. پیش از تکمیل این تصویر، تحقیقات بیشتری باید توسط گروههای مختلف انجام شود». چه کسی میتواند با این حرف مخالفت کند؟